暖等离子体合成过渡金属掺杂氧化锰析氧电催化剂
李家琪, 李小松, 李煊赫, 朱晓兵, 朱爱民
无机材料学报
2024, 39 ( 7):
835-844.
DOI:10.15541/jim20230542
可再生能源发电与质子交换膜水电解结合产生“绿色氢”对能源安全具有战略意义, 其速控步骤是析氧反应。从稳定性、活性和成本角度考虑, 本研究采用滑动弧暖等离子体一步合成了氧化锰(MnOx)及过渡金属掺杂(Fe-MnOx, Co-MnOx, Ni-MnOx)的析氧电催化剂, 并对其晶体结构、形貌尺寸、元素组成和表面价态进行了表征。氧化锰主要由晶相Mn2O3和无定形Mn3O4组成。与之相比, 掺杂的氧化锰尽管晶相组成基本不变, 但其粒径明显变小、比表面积增大; 掺杂Co促使氧化锰的表面电子增多。氧化锰基催化剂在酸性电解液的循环伏安测试中表现出独特的电流阶跃现象(低电势Ⅰ-Ⅱ区: 1.4~1.8~2.4 V; 高电势Ⅲ区: 2.4~2.7 V)。该电流阶跃过程与Bulter-Volmer简化方程的电极动力学参照曲线相吻合, 属于多价态锰参与的电催化反应。低电势区Fe-MnOx的电化学活性最优, 而高电势区Co-MnOx表现最优。Co-MnOx的起始电位比MnOx低160 mV, 且在恒电位电解中其末端电流密度是MnOx的3倍。与其活性趋势一致, Fe-MnOx、Co-MnOx分别在低电势区、高电势区更具稳定性。本研究通过掺杂过渡金属优化氧化锰的颗粒尺寸、比表面积和电子结构, 显著提高了催化剂析氧反应活性及稳定性。
View image in article
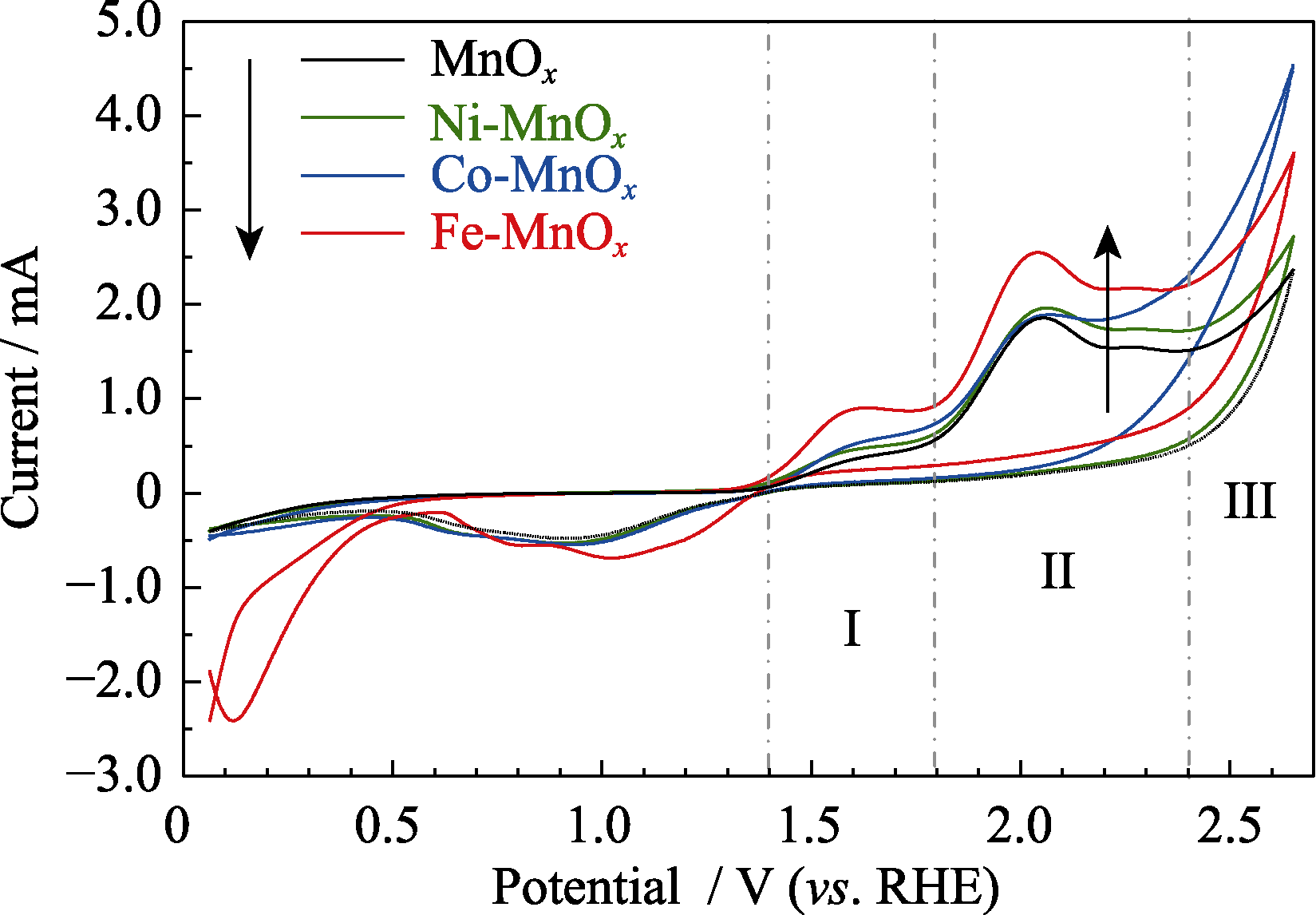
图4
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的循环伏安曲线
正文中引用本图/表的段落
为了对比暖等离子体制备的MnOx及其过渡金属掺杂型催化剂(Ni-MnOx、Co-MnOx和Fe-MnOx)的电化学性能, 首先, 在酸性电解液(0.1 mol·L-1 H2SO4)中测试CV曲线, 结果见图4。有趣的是, 滑动弧暖等离子体合成的四种催化剂均出现了三次(连续性)电流阶跃现象。这是首次发现氧化锰在酸性电解液中的阶跃行为。电流阶跃过程所对应的电压区间可划分为I区(1.4~1.8 V), Ⅱ区(1.8~2.4 V), Ⅲ区(2.4~2.7 V)。从起始电位角度分析, 四种催化剂在I区和Ⅱ区的起始电位相近。值得注意的是, Co-MnOx在Ⅲ区具有更低的起始电位, 比MnOx低160 mV。从氧化电流方面分析, 在I区和Ⅱ区, 同一电压下Fe-MnOx的电流较高。尤其是Fe-MnOx在2.04 V的电流高达2.55 mA, 是MnOx的近1.4倍。在III区, 电压超过2.4 V后Co-MnOx的电流大幅度上升。Co-MnOx在2.65 V的电流高达4.53 mA, 是MnOx的约1.9倍。
由于四种催化剂在氧化过程中存在阶跃现象, 本研究设计了不同截止电压的CV测试, 以便清晰地认识该阶跃过程。不同截止电压的CV曲线见图5(a~e)和图S4。同时, 结合热力学平衡电势, 推断每段阶跃可能发生的过程, 具体反应式见补充材料[46]。I区的CV曲线重合较好, 表明此过程中高价态锰未发生溶解, 推测I区发生的反应为Mn2+氧化成Mn3+; Ⅱ区初始阶段CV曲线不同圈数重合较好, 推测其反应为Mn2+氧化为Mn4+, 但随着电压增大(>2.0 V), 电流出现衰减, 表明在此电压下, 催化剂遭到破坏, 生成MnO42-并少部分溶解在电解液中, 使得催化剂活性降低; 同样, Ⅲ区主要为Mn2+氧化为MnO4-以及MnO42-氧化为MnO4-。图5(f)为根据经验公式得到的氧化锰CV拟合曲线与测试曲线。该经验公式如下[47-48]:
从双电层角度进一步解释电流阶跃特征(图4和图5)。在阳极发生的析氧反应中, 重点考虑双电层处的电子转移(图9)。双电层由固体(MnOx催化剂)和溶液两侧组成。由于MnOx是一种具有多价态和多相态的化合物, 这种价态可变化性可以促进锰较快地失去电子(从低价态变成高价态, 红色箭头)。与之对应的是, 溶液侧的反应物水发生氧化而较慢地失去电子(这些电子穿隧双电层至另一侧的高价锰(蓝色箭头))及生成质子和氧气。因此, 就电子转移的本征速率而言, 双电层(固体和溶液)两侧的显著差异性以及锰的多价态可变化性, 必然导致在双电层两侧快速或慢速的电子转移过程, 综合表现为阶跃式的电流特征。该电极动力学过程中, 微观局域可能出现暂态不均衡的电荷力, 但材料应力会自适应达到暂态平衡。值得强调的是, 这种锰价态变化能够促进反应中氧物种的吸附和解离, 形成多个子步骤, 提供多种可能的反应路径, 从而降低活化能[51]。
本文的其它图/表
-
 表1
采用ICP-OES, BET, XRD, TEM表征MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的物理化学参数
表1
采用ICP-OES, BET, XRD, TEM表征MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的物理化学参数
-
 图S1
滑动弧暖等离子体合成的氧化锰基催化剂的形貌照片
图S1
滑动弧暖等离子体合成的氧化锰基催化剂的形貌照片
-
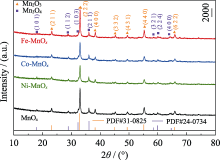 图1
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的XRD谱图
图1
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的XRD谱图
-
 图2
(a, e)MnOx, (b, f)Ni-MnOx, (c, g)Co-MnOx和(d, h)Fe-MnOx催化剂的(a~d)TEM和(e~h)HRTEM照片((a~d)中的插图为相应的颗粒粒径分布直方图)
图2
(a, e)MnOx, (b, f)Ni-MnOx, (c, g)Co-MnOx和(d, h)Fe-MnOx催化剂的(a~d)TEM和(e~h)HRTEM照片((a~d)中的插图为相应的颗粒粒径分布直方图)
-
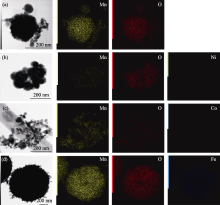 图S2
氧化锰基催化剂的元素能谱分布(EDX)图
图S2
氧化锰基催化剂的元素能谱分布(EDX)图
-
 图3
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的(a)Mn2p和(b)O1s XPS谱图
图3
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的(a)Mn2p和(b)O1s XPS谱图
-
 图S3
Ni-MnOx催化剂的(a)Ni2p, Co-MnOx催化剂的(b)Co2p和Fe-MnOx催化剂的(c)Fe2p XPS谱图
图S3
Ni-MnOx催化剂的(a)Ni2p, Co-MnOx催化剂的(b)Co2p和Fe-MnOx催化剂的(c)Fe2p XPS谱图
-
 图5
滑动弧暖等离子体合成MnOx催化剂在截止电压为(a)1.5, (b)1.7, (c)1.9, (d)2.3, (e)2.6 V的CV曲线, (f)CV的测试和拟合曲线
图5
滑动弧暖等离子体合成MnOx催化剂在截止电压为(a)1.5, (b)1.7, (c)1.9, (d)2.3, (e)2.6 V的CV曲线, (f)CV的测试和拟合曲线
-
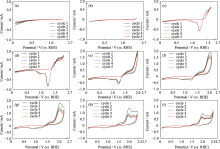 图S4
滑动弧暖等离子体合成MnOx催化剂在不同截止电压(a)1.3, (b)1.4, (c)1.6, (d)1.8, (e)2.0, (f)2.1, (g)2.2, (h)2.4和(i)2.5 V的循环伏安图
图S4
滑动弧暖等离子体合成MnOx催化剂在不同截止电压(a)1.3, (b)1.4, (c)1.6, (d)1.8, (e)2.0, (f)2.1, (g)2.2, (h)2.4和(i)2.5 V的循环伏安图
-
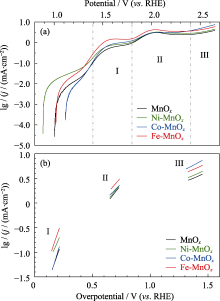 图6
MnOx、Ni-MnOx、Co-MnOx和Fe-MnOx催化剂的(a)lgj-E曲线和(b)类Tafel斜率图
图6
MnOx、Ni-MnOx、Co-MnOx和Fe-MnOx催化剂的(a)lgj-E曲线和(b)类Tafel斜率图
-
 表S1
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的电化学性能(源自图6)
表S1
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的电化学性能(源自图6)
-
 图S5
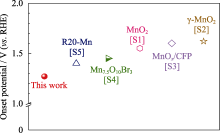
三维多孔电极中Co-MnOx催化剂与文献[S1-S5]报道的二维薄膜电极中氧化锰基催化剂在酸性条件下的析氧反应起始电位比较
图S5
三维多孔电极中Co-MnOx催化剂与文献[S1-S5]报道的二维薄膜电极中氧化锰基催化剂在酸性条件下的析氧反应起始电位比较
-
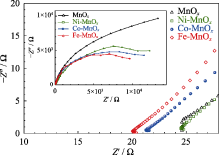 图7
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的电化学阻抗谱图(插图为所测全部频率谱图)
图7
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂的电化学阻抗谱图(插图为所测全部频率谱图)
-
 图8
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂在(a, d)1.5, (b, e) 1.9和(c, f) 2.5 V电压下的(a~c)电流密度-时间(j-t)的稳定性实验, 以及(d~f)电流衰减率与上述稳定性实验的末端电流密度的关系
图8
MnOx, Ni-MnOx, Co-MnOx和Fe-MnOx催化剂在(a, d)1.5, (b, e) 1.9和(c, f) 2.5 V电压下的(a~c)电流密度-时间(j-t)的稳定性实验, 以及(d~f)电流衰减率与上述稳定性实验的末端电流密度的关系
-
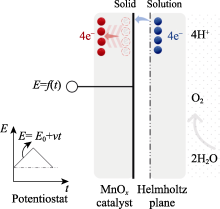 图9
电流阶跃特征的双电层解释示意图
图9
电流阶跃特征的双电层解释示意图
|